当前位置:
查字典高考网 > 高考资讯 > 综合资讯 > 【每日一题】原电池原理
【每日一题】原电池原理
发布时间: 2017-04-30 来源:查字典高考网
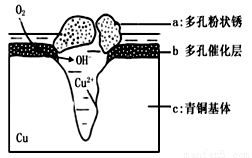
青铜器的制造是中华民族劳动人民智慧的结晶,成为一个时代的象征,但出土的青铜器大多受到环境腐蚀。如图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。环境中的 Cl-扩散到孔口,并与各电极产物作用生成多孔粉状锈 Cu2(OH)3Cl 。
下列说法不正确的是( )
A. 腐蚀过程中,负极 a被氧化
B. 环境中的Cl-扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl,其离子方程式为2Cu2++3OH-+Cl-=Cu2(OH)3Cl↓
C. 若生成 2.145gCu2(OH)3Cl,则理论上消耗标准状况氧气体积为 0.448L
D. 正极的电极反应式为:正极反应是 O2+ 4e-+2H2O=4OH-
答案与解析
解析:A、根据图知,氧气得电子生成氢氧根离子、Cu失电子生成铜离子,发生吸氧腐蚀,则Cu作负极被氧化,腐蚀过程中,负极是a,A正确;B、Cl-扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl,负极上生成铜离子、正极上生成氢氧根离子,所以该离子反应为氯离子、铜离子和氢氧根离子反应生成Cu2(OH)3Cl沉淀,离子方程式为2Cu2++3OH-+Cl-=Cu2(OH)3Cl↓,B正确;C、n[Cu2(OH)3Cl]=2.145g214.5g/mol=0.01mol,根据转移电子相等可得n(O2)=0.01mol22/4=0.01mol,故在标准状态体积为V=0.01mol22.4L/mol=0.224L,C错误;D、氧气在正极得电子生成氢氧根离子,电极反应式为:O2+ 4e-+2H2O=4OH-,D正确。
答案:
C
查看全部
大家都在看
- 高校实行自主招生 高中生如何应对新入学模式
- 复旦上海交大自主选拔方案敲定 先过“海选”关
- 复旦自主招生复试:三大变化甄选优秀人才
- 厦门大学保送生和自主招生申请截止时间推迟
- 复旦大学07年自主招生三个启示
- 厦门大学保送生自主招生人选务必于今日前确认
- 哈尔滨工业大学07年首次自主招生测试开始
- 15分钟成了最大的心理障碍--复旦大学自主招生面试解析
- 湖北经济学院自主招生开始 不面试只笔试
- 让面试思如泉涌--我参加自主招生的经历
- 听清华北大复旦招生负责人谈眼里的优秀生
- 中国海洋大学自主招生考试不分文理
- 复旦面试:热点问题考查学生责任感
- 政策全剖析--2007年全国普通高考报考指南(1)
- 复旦自主招生面试 考官和学生侃起牛市
- 虚假“保送生”取消高考资格
- 直面自己--上海交通大学自主招生面试解析
- 山东省2007年高考保送生政策出台
- 我如何搞定复旦大学自主招生面试
- 从兴趣入手!上海交大自主招生精彩问答集锦
- 2006届清华大学自主招生数学试题
- 上海11校参加专科层次依法自主招生改革试点
- 复旦大学特招生:大学生活让他们很快乐
- 复旦、交大公布2007年自主选拔录取改革方案
- 越亲切的老师越有“杀伤力”--复旦大学自主招生面试解析
- 中学如何配合高校自主招生
- 四川07年普通高等学校招收保送生工作通知
- 河南学子北大归来畅谈体验自主招生
- 南京大学07自主招生面试:时政题多 学生知识面窄
- 自主选拔录取学生的共性